- Фотографічні властивості [ правити | правити код ]
- антиоксидант [ правити | правити код ]
- Розрив ланцюга полімеризації [ правити | правити код ]
- Знебарвлюючий агент [ правити | правити код ]
- Підтримка активності прояви [ правити | правити код ]
open wikipedia design.
сульфіт натрію  <
< 
 Хім. формула Na2SO3 молярна маса 126,037 г / моль щільність 2,633 г / см³ Т. плав. 500 ° C [1] 600 ° C [1] розчинність в воді 14,29 г / 100 мл (0 ° С)
Хім. формула Na2SO3 молярна маса 126,037 г / моль щільність 2,633 г / см³ Т. плав. 500 ° C [1] 600 ° C [1] розчинність в воді 14,29 г / 100 мл (0 ° С)
26,10 г / 100 мл (20 ° С)
36,99 г / 100 мл (40 ° С)
29,20 г / 100 мл (80 ° С) Реєстр. номер CAS 7757-83-7 PubChem 24437 Реєстр. номер EINECS 231-821-4 SMILES InChI Кодекс Аліментаріус E221 RTECS WE2150000 ChEBI 86477 ChemSpider 22845 токсичність помірна Наводяться дані для стандартних умов (25 ° C, 100 кПа) , Якщо не вказано іншого.
Сульфіт натрію (серністокіслий натрій) - неорганічне з'єднання , сіль натрію і сірчистої кислоти з формулою Na2SO3. Застосовують у фотографії, при виготовленні тканин і віскози, при обробці руд кольорових металів і для знешкодження стічних вод.
У фотографії вперше було використано в 1882 році Х. Б. Берклі для пірогаллолових проявителей з метою зменшити плями, що виникають на фотоматеріалі в процесі обробки. З 1882 року багато склади включали в себе сульфітні іони, як правило з цілями захисту проявника від окислення, але в цілому роль цих іонів була малозрозуміла і тільки через роки досліджень вдалося виявити значний ряд функцій цього з'єднання в складі виявляють розчинів [2] .
З'єднання має вигляд безбарвних кристалів гексагональної сингонії з параметрами: a = 0,5459 нм, с = 0,6160 нм, z = 2, просторова група C3. Щільність 2,633 г / см3. Розчинний у воді, при цьому з ростом температури розчинність спочатку зростає (в 100 г води): 14,29 г (при 0 ° C), 26,10 г (при 20 ° C), 36,99 г (при 40 ° C ), далі падає: 29,20 г (при 80 ° C). Межа температури, після якої починається зменшення розчинності і початок кристалізації - 33,4 ° C [3] .
Утворює гептагідрат Na2SO3 · 7H2O при кристалізації з водних розчинів нижче 33,4 ° C. Гептагідрат сульфіту натрію має щільність 1,539 г / см3 [3] .
Сульфіт натрію стійкий на повітрі при кімнатній температурі, але при нагріванні розкладається з утворенням сульфату натрію і сульфіду натрію , При цьому при температурі вище 800 ° C розкладання йде до утворення оксиду натрію і діоксиду сірки [3] .
Гептагідрат сульфіту натрію у вологому повітрі легко окислюється до сульфату натрію, для уповільнення окислення використовують інгібітори - гідрохінон , пирогаллол , 1,4-фенілендіамін . У сухому повітрі гептагідрат що не окислюється, але частково втрачає кристалізаційну воду, повністю зневоднюючи при температурі 150-160 ° C [3] .
Водні розчини сульфіту натрію мають лужну реакцію, при їх подкислении відбувається виділення діоксиду сірки [4] .
Сульфіт натрію є сильним відновником. У водних розчинах знаходиться в частково гідролізованому стані, легко окислюється киснем повітря, перманганатом калію , біхроматом калію , бромом , йодом і іншими окислювачами до сульфату натрію. Розчини сульфіту натрію поглинають діоксид сірки, утворюючи гідросульфіт натрію , А при кип'ятінні приєднують сірку з освітою тіосульфату натрію . У кислих розчинах хлориду титану (III) , двуххлорістого олова і хлориду заліза (II) відновлюється до Дитіоніти натрію або до сульфіду натрію [3] .
Фотографічні властивості [ правити | правити код ]
Численні дослідження властивостей сульфіту натрію в складі виявляють розчинів показали, що дія цього з'єднання не обмежується вузькою областю зниження кількості плям на емульсії, що утворюються в процесі обробки в деяких фарбувальних проявителях, для чого це з'єднання було запропоновано спочатку. Практично відразу сульфіт натрію став використовуватися в своїй ролі основного універсального зберігає речовини, що було викликано його багатоаспектним дією на фотографічні склади при всіх етапах прояву і зберігання розчинів [5] .
антиоксидант [ правити | правити код ]
Основна роль сульфіту натрію в складі фотографічних виявляють розчинів полягає в захисті органічних виявили речовин від окислення киснем повітря. При високому значенні pH розчину виявляючи речовина в відсутності сульфіту швидко окислюється, стаючи фотографічно неактивним. Наприклад, гідрохінон спочатку перетворюється в хинон , Внаслідок чого розчин набуває жовте забарвлення, а потім в фотографічно неактивний оксіхінон, що забарвлює розчин в темно-коричневий колір. Невелика кількість сульфіту натрію різко уповільнює цей процес за рахунок того, що замість гидрохинона з киснем в першу чергу буде реагувати сам сульфит з утворенням сульфату натрію. Присутність же органічного виявляє речовини, в свою чергу, є інгібітором процесу окислення сульфіту киснем [7] .
Точний механізм інгібування окислення органічних виявили речовин невідомий, але передбачається, що він обумовлений зв'язуванням сульфитом натрію забарвлених окислених форм виявили речовин, які в незв'язаному стані каталізують подальше окислення своєї неокисленого форми [7] .
Окислення гидрохинона киснем повітря в розчинах, що містять сульфіт натрію, буде відбуватися вже не з утворенням хинона і оксіхінона, а з утворенням безбарвного добезілат натрію, який також є виявляють речовиною [7] :
![Окислення гидрохинона киснем повітря в розчинах, що містять сульфіт натрію, буде відбуватися вже не з утворенням хинона і оксіхінона, а з утворенням безбарвного добезілат натрію, який також є виявляють речовиною [7] :](/wp-content/uploads/2019/12/uk-wikizero-sulfit-natriu-4.png)
+ O2 + 2 Na2SO3 → H 2 O {\ displaystyle {\ ce {-> [H_ {2} O]}}} 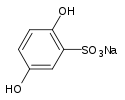 + Na2SO4 + NaOH
+ Na2SO4 + NaOH
Розрив ланцюга полімеризації [ правити | правити код ]
При прояві гидрохиноном і його похідними в розчині утворюються семіхінонов - високоактивні і нестабільні з'єднання. Вони мають тенденцію до полімеризації в гумінові кислоти , Ланцюги яких в типових умовах для фотографічного прояву утворюються з близько 10 молекул окислених залишків гидрохинона і мають темне забарвлення. Так як на стадії освіти семіхінонов сульфит реагує з ним, то полімеризації, як правило, не відбувається, а отже, не буде і каталітичного впливу даних полімерних з'єднань на неокислену форму виявляє речовини. Проте, для пирогаллола сульфит не здатний взаємодіяти з нерозчинними забарвленими продуктами окислення, аналогічно і для слабоокрашенних продуктів окислення фенидона і L-аскорбінової кислоти [5] .
Знебарвлюючий агент [ правити | правити код ]
Сульфіт натрію в описаному вище процесі зв'язування забарвлених форм утворює безбарвні з'єднання, замість сільноокрашенних, тим самим знижуючи небажані плями і забарвлення результуючого зображення [5] .
Підтримка активності прояви [ правити | правити код ]
Окислені залишки виявляє речовини в розчині, хоча і безпосередньо не реагують з галогенідів срібла в емульсії, але змінюють pH середовища та інші її показники, що може вести або до наростання швидкості прояви, або до її спаду. Лише деякі виявляють речовини не дають подібного ефекту. Зростання активності спостерігається в пропрацювали розчинах виявляють речовин, що мають активні гидроксогрупп, наприклад у гліцину-фото . Якщо ж проявляє речовина має лише аміногрупи, то швидкість прояви падатиме. Перетворення окислених форм в сульфонати при реакції з сульфитом стабілізує і підтримує активність, тим самим дозволяючи уникнути небажаного пере- або недопроявленія [5] .
Сульфіт натрію отримують:
- взаємодією розчинів Na2CO3 з SO2 :
N a 2 CO 3 + SO 2 → N a 2 SO 3 + CO 2 {\ displaystyle {\ mathsf {Na_ {2} CO_ {3} + SO_ {2} \ rightarrow Na_ {2} SO_ {3} + CO_ { 2}}}} N a H S O 3 + N a O H → N a 2 S O 3 + H 2 O {\ displaystyle {\ mathsf {NaHSO_ {3} + NaOH \ rightarrow Na_ {2} SO_ {3} + H_ {2} O}}}
2 N a O H + S O 2 → N a 2 S O 3 + H 2 O {\ displaystyle {\ mathsf {2NaOH + SO_ {2} \ rightarrow Na_ {2} SO_ {3} + H_ {2} O}}}
Безводну сіль:
2 NaHSO 3 + Ca (OH) 2 ⟶ CaSO 3 ↓ + Na 2 SO 3 + 2 H 2 O {\ displaystyle {\ ce {2NaHSO3 + Ca (OH) 2 -> CaSO3v + Na2SO3 + 2H2O}}}
Застосовують для видалення слідів хлору після відбілювання тканин, для видалення сірки з віскози після формування, як флотореагент для руд кольорових металів, у виробництві пестицидів , Для знешкодження стічних вод, що містять хром [3] .
У фотографії використовують як основне зберігає речовину в проявителях , Входить до складу фіксажів і інших розчинів [8] [3] .
Тимчасово припустима концентрація в повітрі 0,1 мг / м3 [3] .
- ↑ 1 2 SODIUM SULFITE
- ↑ Haist, 1979 , С. 220.
- ↑ 1 2 3 4 5 6 7 8 Білоусова, 1992 .
- ↑ Стасіневіч, 1964 .
- ↑ 1 2 3 4 5 Haist, 1979 , С. 220-229.
- ↑ Редько, 2006 , С. 857.
- ↑ 1 2 3 Редько, 2006 , С. 856.
- ↑ Гурлев, 1988 , С. 296.
- Білоусова А. П. Натрію сульфіт: стаття // Хімічна енциклопедія / Гол. ред. Кнунянц І. Л . - М.: Велика Російська енциклопедія , 1992. - Т. 3: Меди - Полімерні. - С. 186. - 639 с. - ISBN 5-85270-039-8 .
- Гурлев Д. С. Довідник по фотографії (обробка фотоматеріалів). - К.: Техніка, 1988. - ISBN 5-335-00125-4 .
- Редько А. В. Хімія фотографічних процесів. - СПб. : НПО "Професіонал", 2006. - С. 837-954. - 1464 с. - (Новий довідник хіміка і технолога / ред. Москвін О. В.; вип. Загальні відомості. Будова речовини. Фізичні властивості найважливіших речовин. Ароматичні сполуки. Хімія фотографічних процесів. Номенклатура органічних сполук. Техніка лабораторних робіт. Основи технології.). - ISBN 978-5-91259-013-9 .
- Стасіневіч Д. С. Натрію сульфіт: стаття // Коротка хімічна енциклопедія / Редкол .: Кнунянц І. Л. (Відп. Ред.) Та ін .. - М.: Радянська енциклопедія , 1964. - Т. 3: Мальтаза-Піроліз. - С. 384.
- Haist GM Modern Photographic Processing. - New York, Chichester, Brisbane, Toronto: John Whiley and sons, 1979. - Т. 1. - (Photographic science and technology and graphic arts). - ISBN 0-471-02228-4 .


